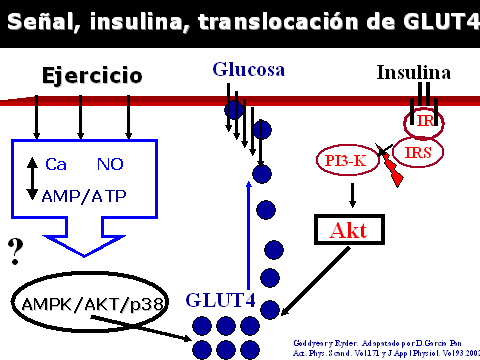
Señales hacia el transporte de glucosa durante
el ejercicio
Como hemos visto
el ejercicio induce de manera independiente del mecanismo de la
insulina, la incorporación y consumo de glucosa por parte del
musculo. Al parecer uno de los mecanismos esenciales esta mediado
por las variaciones en las concentraciones del Ca por intermedio de
la activación de otra proteína kinasa, denominada C (PKC) que
involucra a AMPK y a otras proteínas que corresponden a la cascada
de señales de insulina como la p38 y la familia de las MAP-kinasas.
En primer lugar
debemos tener en claro que en los fenómenos macro del consumo de
glucosa por parte del musculo están involucrados los procesos de
aumento del aporte de glucosa a la membrana celular debido al
aumento de la capilaridad y perfusión que involucra el ejercicio y
seguidamente por el incremento de la capacidad de transporte de la
membrana obtenido por la vía de translocación de los GLUT4 y por los
micro-tùbulos que los trasladan desde el espacio intracelular a la
membrana. Hasta la fecha se ha podido constatar que el Ca juega un
rol importante en la sensibilización de la célula por el consumo de
glucosa, sin embargo los mecanismos por los cuales se produce esta
sensibilización no están aun claros. Por otro lado también se ha
visto que AMPK juega un rol ya que sin su presencia no son tan
evidentes los efectos de los cambios de concentración de Ca por si
solo y una vez mas el efecto esta supeditado al nivel de los
depósitos de glicógeno intramuscular.(12)
Los experimentos
incluyen los efectos farmacológicos de inducción de un incremento
del calcio mioplasmico lo que a su vez produce un incremento del
transporte de glucosa hacia el musculo y también una vez mas este
transporte de glucosa es dependiente de la frecuencia e intensidad
de las contracciones.
también PKC es
activada gracias a que en la contracción repetida del musculo se
incorporan diagliceroles los que inhiben la cascada de señales de
insulina y por lo tanto es una proteína moderadora de la entrada de
glucosa al citoplasma celular. Pero en todos los fenómenos de
incorporación de mayor o menor glucosa al musculo es dependiente de
la actividad de AMPK la cual a su vez es dependiente de los niveles
de depósitos de glicógeno como lo hemos visto anteriormente
(13).
La dispersión en los modelos experimentales tampoco permiten tener
un consenso al respecto ya que independiente de los niveles de
glicógeno se ha podido observar una igual actividad por parte de
AMPK
(14).
Se ha podido
constatar que en reposo el musculo es dependiente del mecanismo de
insulina para la incorporación de glucosa, se han visto involucradas
otras proteínas como las mitogeno-activadas proteínas kinasas (MAPK),
la p38, JNK y ERK , sin embargo en el musculo sometido a
contracciones, al parecer el estimulo del ejercicio pasa o se salta
a estas proteínas, no adjudicándole un rol en el consumo de glucosa
por parte del músculo durante el ejercicio.(15)
Todo estas
observaciones nos permiten concluir que los cambios de las
concentraciones de Ca intracelular en el musculo esquelético durante
el ejercicio juegan un rol en complicidad con AMPK y dejan de lado
una serie de otras proteínas que conforman parte de la cascada de
señales de insulina, lo que agrega un factor potenciador del
ejercicio en la regulación de los niveles de glicemia.
Activación de GLUT4
En las secciones
anteriores nombramos a los transportadores de glucosa GLUT4. Como es
sabido Glut4 pertenece a una familia de 10 GLUT siendo GLUT 4 el
transportador de glucosa del plasma al interior de la célula del
tejido adiposo y muscular. Por lo tanto GLUT4 es el principal
transportador de glucosa y en definitiva los mecanismos de insulina
están destinado básicamente a activar estos GLUT 4 para hacer
posible el consumo de glucosa por parte de dichas células, es decir,
adiposa y muscular. Ya en la década del 70, se demostró en membranas
aisladas que las estimuladas con insulina reunía una significativa
mayor concentración de GLUT 4 que las no estimuladas. Se han
definido dos mecanismos de la insulina para poder llevar a cabo esta
acción.
La primera es la
acción de reclutar los transportadores desde las reservas
intracelulares e insertarlas en la membrana plasmática. Una segunda
actividad importante también ya que es relativa a los niveles
mayores de stress al que se somete a la célula, es la de aumentar la
actividad intrínseca de estos transportadores. La señal de insulina,
como bien sabemos, es una cascada que pasa por varias proteínas
kinasas o proteínas señales y que van a ser moderadoras y
moduladoras de los consiguientes estímulos de la insulina, entre
ellas la mas importante detectada hasta la fecha es la p38 MAPK (mitogeno
activated protein kinasa). La necesidad de modulación es necesaria
ya que se han encontrado hasta incrementos de 100 veces mas de GLUT4
en células estimuladas al máximo con insulina. Este aumento guarda
relación con los miotubulos y también con la posterior translocación
de los GLUT4. La eficiencia de la insulina depende básicamente de la
activación de los transportadores y esta también es estimulada en
primer termino por el cambio de temperatura antes que el estimulo de
la insulina propiamente tal.(16)
La p38, como
mediador de este estimulo de insulina, es sensible a la hypoxia, a
los radicales libres, a la hipertonicidad, a los rayos ultra violeta
y a los inhibidores de la síntesis de proteinas, mecanismos
coincidentes y también en parte dependientes de AMPK. Los protocolos
experimentales de inhibición y estimulación de esta proteína, p38,
asi lo demuestran dejando en evidencia que p38 MAPK por si sola
también incrementan la actividad intrínseca de GLUT4 en células
adiposas y musculares. Desde la aplicación de insulina sobre un
grupo de estas células ya sea por vía de PKB/Akt y PKC o por p38
MAPK poseen una diferencia de tiempo en la translocación y en la
activación de GLUT4 siendo mas rápida por la primera via que por
p38. La llegada a la membrana plasmatica de estos transportadores
desde el comienzo del estimulo de insulina es de una media de 6
minutos.
Podemos deducir
que los transportadores de glucosa al interior de la célula muscular
poseen una actividad que esta acondicionada a la calidad del
estimulo de insulina y esta calidad a su vez acondicionada a la
actividad de una serie de proteínas kinasas que conforman la cascada
de señales de insulina. También estas proteínas kinasas cambian su
actividad dependiendo de varios factores que son provocados por el
stress celular y que en nuestro interés, el ejercicio, presenta
cambios en las variables rígidas intracelulares como temperatura y
pH las que van servir de estimulo adicional para la translocación,
activación y transporte de los GLUT4.
Regulacion y metabolismo de las grasas en
reposo y ejercicio.
Hemos abordado
los mecanismos intracelulares que promueven el consumo de glucosa
por parte del musculo, teniendo en cuenta que hiperglicemia y
consiguiente hiperinsulinemia dan paso a la insulino resistencia y
así se deriva al síndrome metabólico que es una de las causas de
morbimortalidad importante en esta primera decada del nuevo siglo.
Una de las correlaciones mas significativas con dichos fenómenos
fisiopatologicos es la obtenida con triglicéridos intramiocelulares
y que en definitiva perturban la cascada de senales de la insulina
haciendo a la célula insulino resistente.
En esta parte
conoceremos los avances científicos en el metabolismo de los
lípidos, donde el lector podrá entender que si bien el tejido
muscular aloja cerca del 80% de la glucosa, también es responsable
de metabolizar una cantidad no despreciable de ácidos grasos,
dejando en evidencia que el tejido muscular es un órgano olvidado
por la medicina ignorando su rol, su origen y sus implicancias en el
equilibrio de múltiples funciones de todo nuestro organismo.
Algunos
conceptos básicos:
Los ácidos grasos son el mayor recurso energético que poseemos tanto
en reposo como en ejercicio. Esto es en forma de deposito y
circulando en el plasma pudiendo esta ultima forma incrementarse de
2 a 4 veces con el ejercicio de moderada intensidad. Un quinto de
este volumen circula en forma de triglicéridos y esta alojado en el
compartimiento intracelular a razón de aproximadamente 2 mmol/kg de
musculo.
En reposos mas o
menos del 30 al 60% de estas grasas son consumidas por el sistema
esplacnico y entre el 15 y el 20% por el tejido muscular, situación
que se revierte dramáticamente durante el ejercicio, ya que su
consumo es aumentado hasta en un 60% por el tejido muscular y
decrece un 15% por el sistema esplacnico.(17)
La relación
entre el acumulo de triglicéridos (Tg) en el sistema muscular y las
alteraciones metabólicas consiguientes son de interés por los
investigadores en el campo de las enfermedades crónicas modernas. La
hidrólisis de los Tg incrementa durante el ejercicio pero aun no
esta claro mediante que mecanismos y mucho menos acerca de como se
regula este consumo.
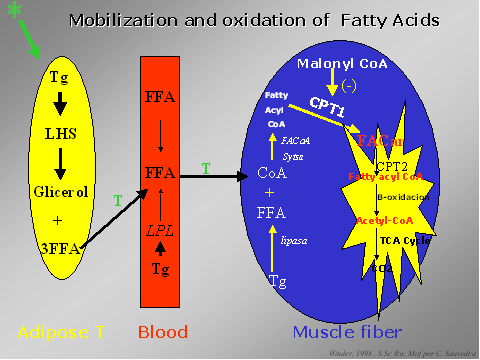
Los modelos
experimentales han podido establecer que en la ausencia de hormonas,
es posible mediante el ejercicio hidrolizar y oxidar dichos Tg,
sugiriéndose por lo tanto de que existen mecanismos intracelulares
responsables de dicho fenómeno. También se ha podido observar que en
el ejercicio moderado tanto los Tg como los ácidos grasos
circulantes aportan proporciones parecidas de lipidos al metabolismo
oxidativa. Ambos fenómenos estan modulados además por la
incorporación de la acción de catecolaminas e insulina y el grado de
entrenamiento del musculo.
El entrenamiento
produce un incremento en la oxidación de ácidos grasos lo cual no
es solo con el aumento del consumo máximo de oxigeno sino que
también con un aumento del umbral, es decir, permite oxidar mas
grasas a intensidades mas altas de ejercicio. Todas estas
apreciaciones y evidencias han sido posible gracias a la actual
tecnología aplicada al estudio del consumo, esterificacion y
oxidación de los lípidos en el tejido muscular.
Normalmente en
reposo le oferta de grasas a los diversos tejidos excede la
capacidad de captación de estos. No olvidemos que el primer recurso
energetico post-absorción para musculo, corazón, hígado y corteza
renal son los ácidos grasos pese a que su cantidad es expresada en
umol/l en el plasma. La vida media de estas grasas circulantes es de
aproximadamente de 3 a 4 minutos en reposo. Este dato es interesante
porque nos da la magnitud de la disponibilidad de la ácidos grasos
ya que pese a ser rapida su desaparición y pese a los bajos niveles
plasmáticos siempre están por sobre las capacidades de extracción
por parte de los diversos órganos y tejidos.
Un valor
promedio post absorción en la noche de grasas circulando es de 5 a 6
umol/kg/min, mientras que la capacidad de oxidación es de 3 a 4 umol/kg/min.
Insulina,
hormona de crecimiento y catecolaminas son los principales
reguladores de este mecanismo ya que por ejemplo insulina puede
inhibir hasta en un 90% los niveles de ácidos grasos circulando
debido a su mecanismo de inhibición de lipólisis. Sin embargo
durante el ejercicio la caída de insulina y el alza de catecolaminas
circulante puede incrementar los valores de ácidos grasos circulante
en 4 a 5 veces.
Los estudios de
la capacidad oxidativa de ácidos grasos están hecho particularmente
utilizando los músculos de las piernas que representan
aproximadamente el 40% de la masa muscular total por lo que la grasa
depositada intramiocelular en esta musculatura podría representar un
40% de la grasa total circulante ya que corazón deposita o consume
el 5% y los riñones el 4%, proporciones que varían
significativamente durante el ejercicio
(18).También
estas proporciones sufren cambios cuando los niveles de ácidos
grasos circulante experimentan cambios, se eleva la proporción de
consumo por parte del musculo y bajan en el lecho. Los datos también
apuntan que no mas del 30% de las grasas ingeridas en 24 horas son
metabolizadas en 24 horas, siendo el resto enviados directamente a
depósitos. Estas proporciones también tienen variaciones en
condiciones de ayuno o de alimentación ya que están reguladas
principalmente por la acción de insulina como dijimos anteriormente
y de glucagon ya sea decreciendo los niveles o aumentándolos
respectivamente. Trasadores e isótopos radioactivos junto con
calorimetrías continuas de 24 horas han permitido hacer este tipo de
seguimiento y estudio, métodos a los cuales aun no se les puede
obtener datos sobre en que tejidos específicamente se oxidan dichos
lípidos.(19)
Aspectos
ligados al entrenamiento:
El
entrenamiento como es sabido, incrementa la posibilidad de
metabolizar u oxidar ácidos grasos gracias al incremento de la
capilaridad del tejido muscular entrenado, de modificar el umbral
oxidativo y ante una misma carga el musculo entrenado puede
modificar la proporción oxidativa de grasas y glicógeno.
Por otro
lado se ha visto que el exceso de glucosa plasmática acompañado de
elevaciones de insulina, inhibe la oxidación de ácidos grasos en el
musculo lo que no sucede a la inversa, es decir ante un aumento de
ácidos grasos circulantes no aumenta la capacidad oxidativa de
grasas por parte del musculo durante el ejercicio.(20)
Esto es muy importante ante los diferentes estados fisiopatológicos
relacionados con insulino resistencia !!
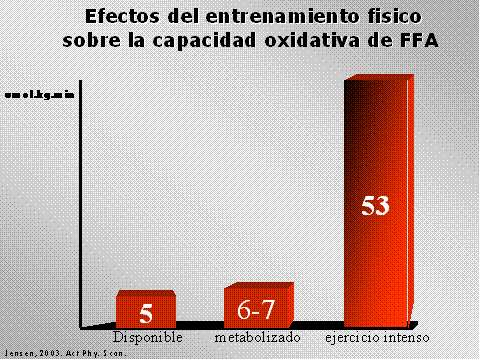
Por otro lado
los estudios llevados a cabos en laboratorios especializados en esta
área del conocimiento han podido constatar que si bien el musculo
entrenado en condiciones de reposo puede exceder el consumo de
grasas en relación a la disponibilidad en umoles/kg/minuto, también
se ha constatado que durante el ejercicio intenso al cual es
sometido un individuo, puede consumir mas grasas que las que tiene
disponible en el torrente sanguíneo suponiéndose así que la
contribución de las grasas o Tg intramusculares aportan de manera
significativa sustratos al metabolismo oxidativo del musculo. De una
disponibilidad de 5 a 6 en reposo puede pasar a una utilización de
53 umol/kg/min que es un valor dos veces mayor que lo que puede
incrementar la disponibilidad en el torrente sanguíneo que circula
por dicho grupo muscular. Sin existir un consenso debido a la
necesidad de perfeccionar las técnicas y los protocolos
experimentales, los laboratorios trabajan intensamente en este campo
debido a que en vitro y en vivo las condiciones y rol de hormonas
juegan papeles importantes que contaminan los resultados y hasta hoy
podemos decir que definitivamente las altas concentraciones de
ácidos grasos extracelular incrementan el flujo de estos al
compartimiento intracelular pero no aumentan la oxidación de estos,
eterificándolos en triglicéridos intramiocelulares.(21)
También, el ejercicio físico incrementa la oxidación de grasas intra
y extracelular
(22)
e incrementa la sintesis de Tg desde el compartimiento extracelular.
(23)
Rol de los lípidos intramusculares y el
SIR.
Como antecedente
importante debemos resumir que el síndrome metabólico es una
expresión de una serie de cuadros fisiopatologicos y que poseen una
raíz común que es el denominado síndrome de insulino resistencia
(SIR). El estudio de los triglicéridos intramiocelulares ha sido una
tarea común en varios laboratorios de investigación debido a que
tanto animales como humanos que poseen SIR también poseen un
incremento en el contenido de los triglicéridos musculares o
intramiocelulares (Tgm).
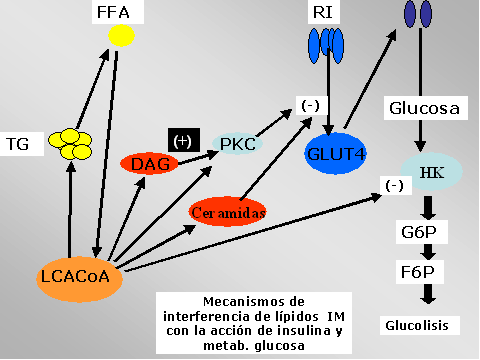
Han sido varios
los lípidos identificados como inhibidores de una serie de proteínas
señales de la cascada de insulina entre los que se encuentran los
propios Tgm , las cerámicas y diacilgliceroles que interfieren en la
señal inhibiendo la actividad de varias enzimas (hexokinasa ,
glicógeno sintetasa) o bien la translocación o activación de
mediadores como es la proteína kinasa C. Todo este cuadro permite
indicar que el exceso de ingesta de lípidos o bien la poca
estimulación de la maquinaria oxidativa mitocondrial de las grasas
serian responsables del SIR lo que también indicaría que la
estimulación de la oxidación de este substrato, permitiría evitar su
acumulación y así también el SIR y que a su vez indicaría ciertas
líneas terapéuticas orientadas a la estimulación del metabolismo
oxidativo de grasas del musculo esquelético.
El musculo
esquelético es responsable del consumo de mas del 80% de la glucosa,
por lo que se le considera un rol importante y una gran
responsabilidad en SIR ya que puede convertirse en el órgano mas
insulino resistente pero también en el mas insulino sensible. El
tejido muscular de pacientes insulino resistentes presenta una
expresión normal de los GLUT4, pero sin embargo una translocación
severamente disminuida de estos desde depósitos intracelulares a la
membrana
(24).
Ya en los anos
60 Randle describió mediante protocolos experimentales adecuados, la
interacción que existe entre lípidos y glucosa en su respectiva
oxidación. En esta descripción se describió claramente que si se
incrementa la cantidad de oxidación de ácidos grasos libres es
posible mediante el incremento de la relación Acetil CoA/CoA, lo que
causa una inhibición de PDH y por consiguiente una disminución de la
producción de ACoA proveniente del piruvato. Por otor lado este
mecanismo produce un incremento del citrato extramitocondrial
provocando una inhibición de PPK, lo que causa una acumulación de
glucosa-6-fosfato inhibiendo la entrada de glucosa en la célula.
Por otro lado la
relación inversa encontrada entre acumulación de lípidos e insulino
sensibilidad ha sido demostrada tanto en sujetos normo peso como
obesos y mediante sofisticados métodos que permiten cuantificar esta
acumulación ya sea mediante biopsias, tomografía computarizada o
resonancia magnética nuclear
(25).
Esto me parece
importante destacar ya que se ha hablado de grasa intramuscular y su
asociación con SIR, ya que por lo general se escucha que las
personas con acumulación de grasa periférica poseen este síndrome
identificando esta grasa con una causa-efecto directa de SIR, sin
embargo hay estudios que demuestran claramente que en situaciones de
lipodistrofia (no producción o acumulación de grasa periférica),
existe grasa intramuscular y consiguiente insulino-resistencia
(26).
La investigación al respecto nos permite afirmar que existe insulino
resistencia en ausencia de niveles elevados de ácidos grasos libres
en el plasma.
Otra evidencia
que ha llevado a una mejor comprensión del rol de los lípidos en el
SIR es el hecho de que una prolongada inhibición vía farmacológica (etomoxir)
de carnitina produce una acumulación de lípidos intramusculares
ocasionando insulino-resistencia incluso reduciendo simultáneamente
los niveles de ácidos grasos en el plasma
(27).
Por otro lado, como veremos mas adelante en esta revisión, se ha
observado un cuadro de insulino-resistencia bien correlacionado con
niveles de MCoA, que es un potente regulador del metabolismo de las
grasas, mediante la inhibición de carnitina-palmitol-transferasa.
Si nos
trasladamos al principio de la cascada de señales de insulina
encontramos también evidencias interesantes que confirman la
necesidad de estimular el metabolismo oxidativo de Tgm.
El aumento de la
actividad de PKC una proteína intermedia de dicha cascada, produce
un aumento de la insulino-resistencia y su inhibición produce el
efecto contrario. Este efecto es concomitante con el aumento de la
actividad de la fosfatil-inositol-3-kinasa. Este fenómeno o
mecanismo ha sido encontrado bien relacionado principalmente con
niveles de ceramidas que es un derivado de esfingomielina que a su
vez es un componente de las membranas celulares. Ceramidas puede
alterar la actividad de kinasas, fosfatasas y la actividad de
trascripción. Los niveles elevados de ceramidas pueden reducir las
capacidad de fosforilación del receptor de insulina, como también la
de PKB constatándose una disminución en la traslocacion de GLUT4.(28)
Es interesante
adquirir la información aparecida entre el fenómeno de SIR y su
interacción con TNF alfa, resistina, leptina, adiponectina, PPAR
gama y alfa que en una u otra dirección tienen potente efectos sobre
la insulino sensibilidad. Leptina por si sola puede aumentar la
insulino sensibilidad mediante mecanismos propios de ella ya que
tiene efectos independientes pudiendo estimular la oxidación de
ácidos grasos en tejidos periféricos y comandar la depleción de
depósitos de grasa. La acción de leptina produciendo una activación
de AMPK no debe ser descartada.
Finalmente es
interesante poder revisar los trabajos de Kelley en que las técnicas
de diferencias arterio-venosa obtenida en diferentes situaciones,
permite comprender las causas de acumulación y desaparición de
ácidos grasos y triglicéridos por parte del musculo esquelético. Una
completa reproducción de sus trabajo pueden obtenerse en una
revisión efectuada por Saavedra,C. y Diaz,X. y publicada en una Guía
Practica de Ejercicio y Alteraciones Metabólicas (2005)
Creo que esta
revisión permite concluir en la necesidad de la estimulación u
oxidación de los ácidos grasos por parte del metabolismo muscular
entendiéndose al ejercicio físico como el fármaco mas efectivo en
dicha estimulación. Esta “prescripcion” permite disminuir el riesgo
de insulino resistencia y alejar las posibilidades de que esta
anormalidad o mecanismo de adaptación para favorecer la oxidación de
los Tgm, derive en el síndrome metabólico que representa hoy en día
un problema prevalente en crecimiento y de importancia para la salud
publica (OMS 1997).
|









